- 首页
- >
- GENESEED
- >
IF39.3!circMPP6还能调控MEX3A和PBs蛋白互作?促癌机制新发现!

2024年4月2日,广东省人民医院乔贵宾主任医师和中山大学谢丹教授、王风华主任医师研究团队在Signal Transduct Target Ther(IF=39.3)上发表文章“Mex-3 RNA binding family member A (MEX3A)/circMPP6 complex promotes colorectal cancer progression by inhibiting autophagy”,该文章明确了在结直肠癌(CRC)中,circMPP6作为介质促进MEX3A和P小体(PBs)蛋白的相互作用,MEX3A/ circMPP6复合物调节PBs的作用,并促进UPF介导的磷酸二酯酶5A (PDE5A)mRNA降解,从而抑制CRC细胞自噬,增强CRC细胞的侵袭性,导致癌细胞恶化,该研究为结直肠癌提供了预后标志和治疗靶点。研究中RIP实验产物的RNA-Seq由吉赛生物提供。
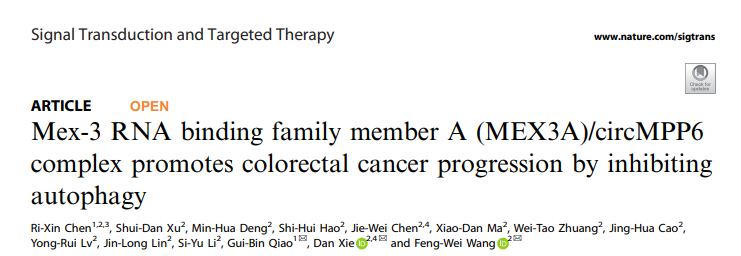
研究思路

主要结果
1、MEX3A在CRCs中高表达,标志预后不良
研究团队使用cBioPortal数据库分析,结合qPCR/WB/IHC对临床样本的检测结果,发现与癌旁组织相比,CRC中MEX3A的表达显著升高。SYSUCC队列显示,CRCs中高表达的MEX3A与临床分期及T、N分期呈正相关,并预示较差的患者总生存期(OS)。这表明,MEX3A的上调在CRC发病机制中具有致癌作用。(图1)
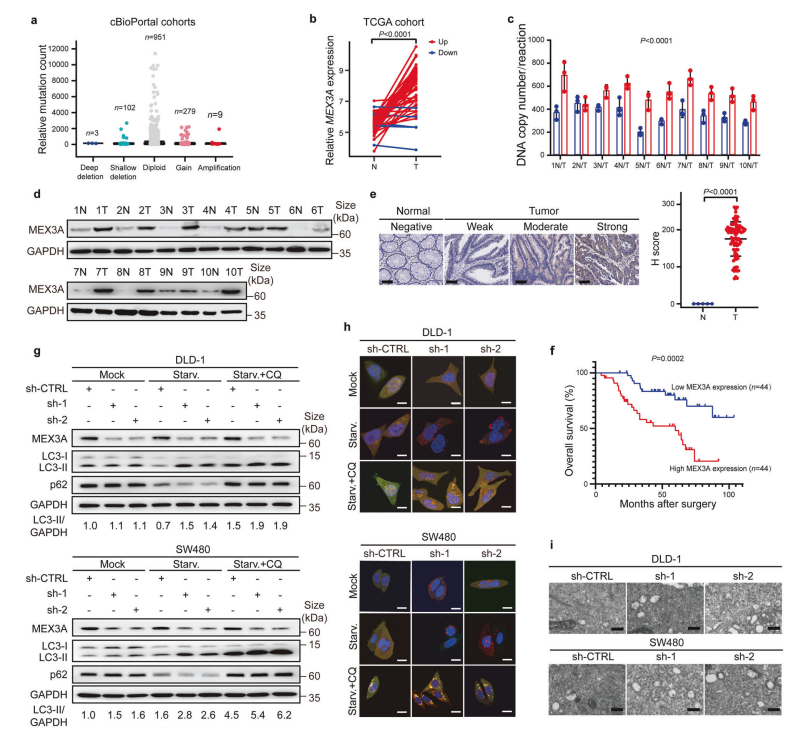
图1. MEX3A在CRC中高表达,抑制CRC细胞的自噬。
2、MEX3A加速CRC细胞的恶化并抑制自噬
研究团队构建MEX3A敲低和过表达结直肠癌稳转细胞株进行实验:体外实验和在体内皮下成瘤实验表明,MEX3A加速了CRC的进展。(图1)
RIP-Seq和KEGG通路分析结果表明,自噬在MEX3A介导的CRC进展中发挥重要作用。(图2)
在血清饥饿时,敲低或过表达MEX3A,检测LC3-II和p62的丰度,结合mRFP-GFP-LC3和透射电镜(TEM)检测,结果表明MEX3A抑制自噬,从而促进结直肠癌的进展。(图2)
研究团队通过构建MEX3A全长序列和两个内在无序区(IDRs)截短突变质粒发现:截短IDRs,液滴大小和数量显著增加;而与全长MEX3A相比,删除IDRs使液滴难以观察到;相分离依赖于温度、蛋白质和盐浓度。(图2)
异位表达EGFP-MEX3A和光脱色荧光恢复(FRAP)实验结果表明,MEX3A的IDRs在CRC肿瘤发生中的LLPS和功能是必需的。(图2)
3、MEX3A与PBs组分之间存在物理相互作用
研究中co-IP和IF实验结果支持了MEX3A蛋白是PBs的一个组成部分。(图2)
图2. MEX3A经历idrs依赖的LLPS,并与PBs组分物理相互作用。
4、MEX3A与circMPP6在PBs中形成复合物
研究通过RIP/RNA-Seq/CircInteractome数据库分析/RT-PCR/Sanger测序/RNase R/放线菌素D实验验证了MOV10结合的circ_0001686(circMPP6);核质分离和FISH实验显示,circMPP6主要定位于细胞质中,呈点状分别。(图3)
研究团队检测了30组结直肠癌组织中circMPP6的表达,发现circMPP6在结直肠癌组织中显著升高。RIP和RNA Pull-down实验证实circMPP6与PBs的核心成分MEX3A和MOV10相互作用。IF-RNA FISH检测发现MEX3A、MOV10和circMPP6在生理条件下在胞质共定位,嘌呤霉素加速circMPP6和MEX3A蛋白向细胞质灶的募集。克隆形成和Transwell迁移实验表明,circMPP6过表达增加了CRC细胞的增殖和迁移能力。在皮下异种移植模型中,circMPP6过表达显著增强了CRC的致瘤性并促进肿瘤生长。这些结果揭示了MEX3A/circMPP6复合物的形成,并表明了MEX3A/circMPP6复合物与CRC细胞中PBs的形成之间的密切关系。(图3)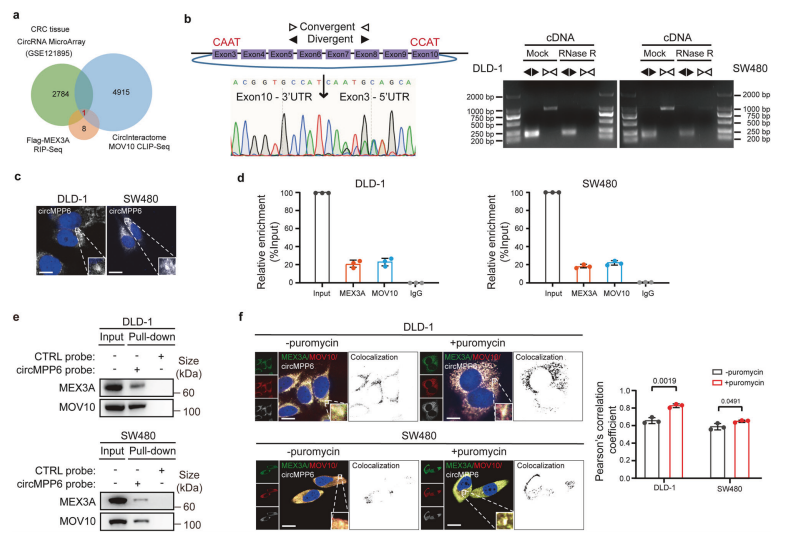
图3. MEX3A与circMPP6在PBs中形成复合物。
5、circMPP6通过加强MEX3A-PBs组分的相互作用促进PBs聚集
WB结果显示circMPP6敲低不影响MEX3A的表达;敲除MEX3A和/或circMPP6后,PBs组分的表达不受影响。IF-RNA FISH检测显示,在嘌呤霉素预处理条件下,缺乏MEX3A和/或circMPP6诱导P小体解离;Co-IP实验结果显示,沉默或RNase A处理circMPP6降低MEX3A免疫沉淀组分中PBs相关蛋白的丰度;蔗糖梯度沉降分离结果表明,MEX3A与PBs蛋白组分的积累依赖于circMPP6。(图4)
该研究通过单独截断异构核核糖核蛋白K同源(KH)结构域,构建了MEX3A突变体。RIP和Co-IP实验结果表明,与circMPP6结合的MEX3A KH2结构域是招募PBs组分所必需的。(图4)
挽救实验显示外源表达的MEX3A野生型(WT),明显逆转沉默MEX3A的促自噬及抑制增殖和转移的作用。这些结果强调了KH2结构域在MEX3A介导的结直肠癌侵袭性中的关键作用。(图4)
作者通过RIP-Seq/RNA Pull-down/RNA- EMSA实验/表型分析证实了CACU基序在circMPP6与MEX3A相互作用中的重要作用及其在CRC发病机制中的功能。这些研究结果表明circMPP6通过影响MEX3A-PBs组分的协作促进PBs聚集和维持。该研究首次阐述了RBP/circRNA复合物与PBs之间的联系。(图5)
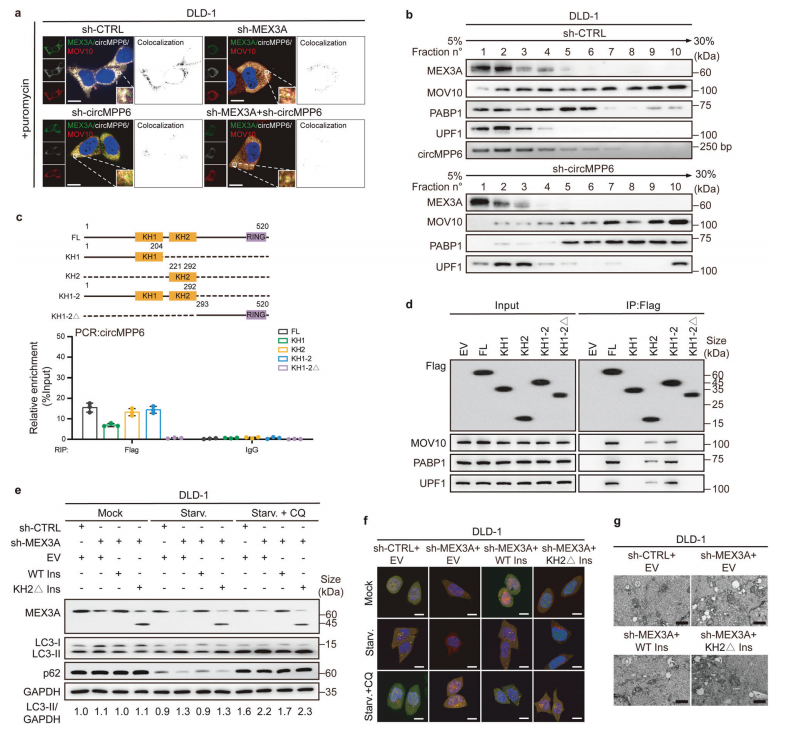
图4. circMPP6通过加强MEX3A-PBs组分的相互作用促进PBs聚集。
6、MEX3A/circMPP6复合物促进PDE5A mRNA的降解
通过对照或敲除MEX3A的DLD-1细胞mRNA-Seq/RIP/RNA Pull-down实验发现PDE5A, SENP7和TTLL7 mRNA受到MEX3A的调控和结合,PBs结构组分MOV10和UPF1表现出招募mRNA的能力。MEX3A/circMPP6敲低后,CRC细胞中PDE5A、SENP7和TTLL7 mRNA的稳定性显著增强。这些结果表明,MEX3A/circMPP6复合物介导的PBs聚集影响mRNA的降解。在MEX3A/circMPP6缺失后,PDE5A蛋白也增加,PDE5A被确定为MEX3A的潜在靶点。(图5)
通过RIP实验,发现MEX3A/ circMPP6敲低显著降低了PDE5A与UPF1的mrna结合能力。IF-RNA FISH检测显示,PDE5A mRNA与UPF1在细胞质中共定位。嘌呤霉素处理降低了PDE5A mRNA的荧光强度。缺乏MEX3A/circMPP6时,UPF1/PDE5A复合物的共定位降低,PDE5A mRNA的荧光强度增加。这些发现PDE5A和UPF1之间MEX3A/circMPP6复合物依赖性相互作用的积累增强了PDE5A mRNA的降解。(图5)
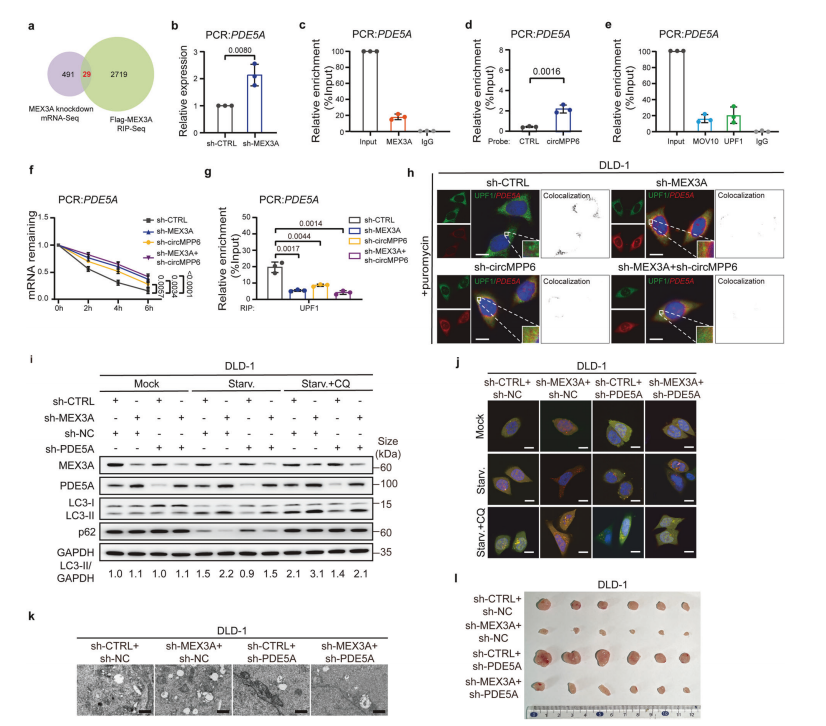
图5. MEX3A/circMPP6复合物促进PDE5A mRNA降解,并通过PDE5A途径调节CRC自噬。
7、MEX3A通过PDE5A途径调控CRC自噬
挽救实验结果表明PDE5A的抑制明显抑制CRC自噬,逆转沉默MEX3A的促自噬作用,显著逆转了MEX3A沉默的对CRC细胞增殖和转移的抑制作用。裸鼠成瘤模型表明,体内PDE5A抑制剂能逆转MEX3A敲低细胞导致的致瘤性降低。裸鼠皮下注射MEX3A敲低或过表达的结直肠癌细胞,检测PDE5A表达发现MEX3A在结直肠癌中的致癌作用依赖于PDE5A通路。(图5)
8、MEX3A/circMPP6-PDE5A轴与CRC进展相关
研究通过TCGA、SYSUCC数据库分析,以及RNA-FISH和IF实验对临床样本的检测,发现PDE5A与MEX3A和circMPP6的表达水平呈负相关。KaplanMeier生存分析表明,高MEX3A和低PDE5A的CRC患者的OS最差。这些结果支持MEX3A上调可显著减弱PDE5A的表达,从而在结直肠癌侵袭性和患者预后中发挥关键作用。(图6)
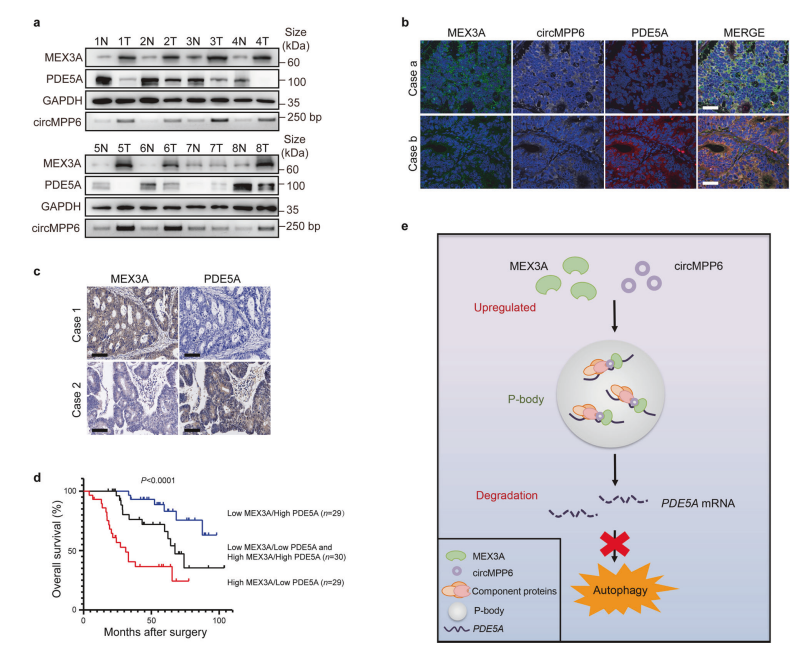
图6. MEX3A/circMPP6-PDE5A轴在临床上与结直肠癌进展相关。
小结
该研究的数据首次描述了MEX3A/circMPP6复合物在调节与结直肠癌发病相关的pbs介导的mRNA衰变中的新功能。该研究的发现揭示了MEX3A诱导肿瘤进展的全新机制,并可能为推进CRC药物治疗提供辅助靶点。
研究中RIP实验产物的RNA-Seq由吉赛生物提供。除常规二代测序服务外,吉赛生物还能提供更出众的三代测序(nanopore纳米孔测序)。Nanopore sequencing 是一种基于纳米孔的单分子实时测序的新一代测序技术。其以单分子DNA通过生物纳米孔的电流变化检测碱基组成而进行测序。
相比二代测序,三代测序具有更强的检出率,更高的灵敏度,更长的读长,更小的误差;能准确识别可变剪切事件,无需拼接,一键生成;能够保留并检测RNA碱基修饰信息,对poly(A)尾长进行相对准确的估算,同时进行全长异构体分析,还原真实RNA特征。三代测序优势明显,发展势不可挡,必将成为分子生物学研究极其重要的技术!