
- 首页
- >
- GENESEED
- >
Nat Commun | 单剂量circRNA疫苗有效预防寨卡病毒感染,而不会增强登革热严重程度
寨卡病毒(ZIKV)与登革热病毒(DENV)在地理分布上有重叠,且两者都属于黄病毒科。ZIKV感染与严重的神经系统疾病有关,包括吉兰-巴雷综合征和新生儿小头症。抗体依赖性增强(ADE)是寨卡病毒(ZIKV)疫苗开发的一个潜在问题。交叉反应而中和性差的抗体通常靶向病毒膜前或包膜(E)蛋白,这可潜在增强登革热病毒(DENV)感染。虽然E结构域III (EDIII)含有寨卡病毒特异性表位,但其免疫原性较差。由于ZIKV和DENV之间的交叉反应性,ZIKV疫苗的开发需要特别注意避免增强DENV感染的ADE效应。
2024年10月16日,中国科学院广州生物医药与健康研究院冯立强研究员、巫林平研究员和陈凌教授在Nature Communications期刊上发表论文:A single-dose circular RNA vaccine prevents Zika virus infection without enhancing dengue severity in mice。研究基于环状RNA(circRNA)开发疫苗,用于预防ZIKV感染,且不增强 DENV的严重性。

该研究表明,与编码单体或三聚体EDIII的circRNA相比,编码融合人IgG1 Fc片段(EDIII-Fc)的二聚体EDIII的circRNA诱导了更好的生发中心反应和更高中和活性的抗体。在免疫C57BL/6小鼠和干扰素α/β受体敲除的成年C57BL/6小鼠中,两剂编码EDIII-Fc和寨卡病毒非结构蛋白NS1(另一种保护性抗原)的circRNA可预防新生儿寨卡病毒的致命感染。重要的是,单剂量优化的circRNA疫苗可改善抗原表达,在小鼠中具有有效和持久的保护作用,而不会诱导明显的DENV ADE,这为基于编码EDIII-Fc和NS1的circRNA开发黄病毒疫苗奠定了基础。
一、EDIII-Fc circRNA具有优于EDIII-Fd或EDIII circRNA的免疫原性
研究设计了三种候选circRNA疫苗,分别编码ZIKV的E蛋白域III(EDIII)的单体、二聚体(与人类IgG1 Fc片段融合,称为EDIII-Fc)和三聚体(与T4噬菌体纤维蛋白的foldon结构域融合,称为EDIII-Fd)。 研究利用鱼腥藻 pre-tRNA(Ana)衍生的Ⅰ型内含子自剪接(PIE)法体外合成circRNA,环化效率超过95%,然后经过HPLC纯化及RNase R处理;将候选疫苗分别转染到HEK293T细胞,验证了EDIII、EDIII-Fc和EDIII-Fd在细胞裂解物中表达相当,而EDIII的分泌效率似乎低于其它两种。(图1) 随后,利用LNP分别包封circRNA候选药物,然后分别肌肉注射到C57BL/6小鼠体内,结果显示EDIII-Fc circRNA比EDIII-Fd和EDIII circRNA引发更高的IgG和nAb滴度,而且EDIII-Fc比EDIII-Fd和EDIII circRNA更能诱导Th1偏向性T细胞反应。综上,与单体和三聚体EDIII相比,二聚体EDIII-Fc circRNA在小鼠中诱导了更好的生发中心反应和更高水平的中和抗体。
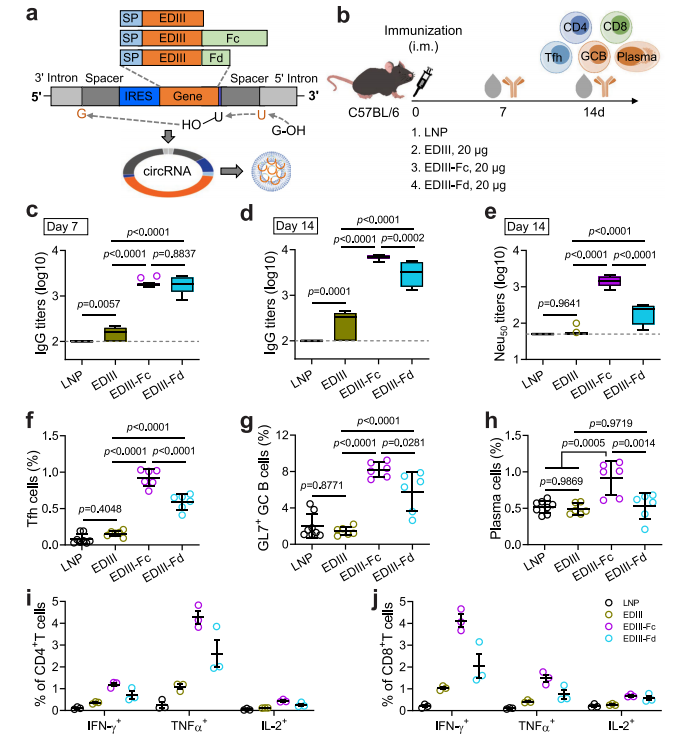
(图1)图1 编码EDIII、EDIII-Fc或EDIII-Fd的circRNA疫苗的免疫原性
二、EDIII-Fc circRNA提供部分保护免受ZIKV感染
在母体被动免疫对新生小鼠的保护作用的评估中,与EDIII-Fd circRNA相比,通过母体免疫EDIII-Fc circRNA可更好地保护后代免受ZIKV攻击。而在circRNA疫苗对成年Ifnar−/− C57BL/6小鼠模型的主动免疫评估中,EDIII-Fc circRNA的降低血清、脑和脾脏中的病毒载量方面比EDIII-Fd circRNA更有效。两种模型中,EDIII-Fc circRNA都提供比EDIII-Fd circRNA更好的保护,但单独使用两者都不足以提供完全的保护。
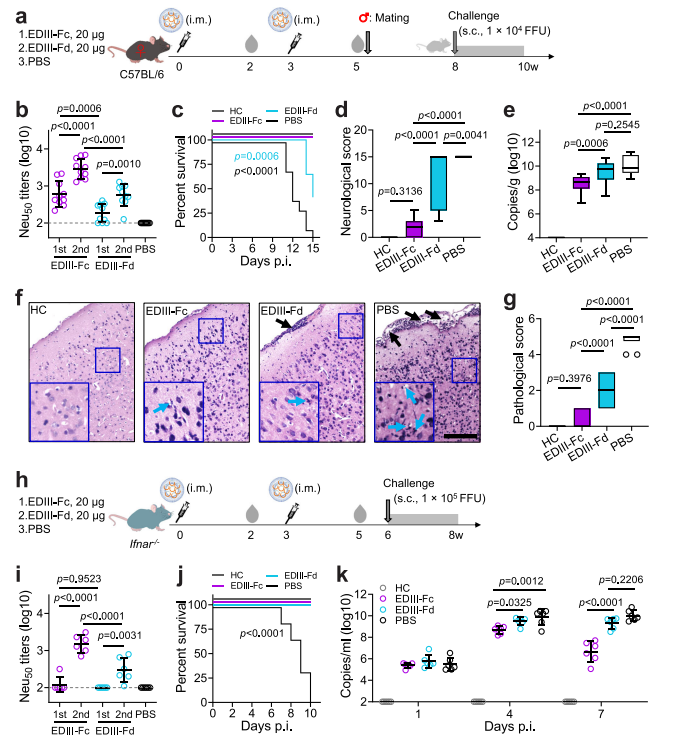
(图2)图2 EDIII-Fc和EDIII-Fd circRNA的保护作用。
三、联合EDIII-Fc和NS1的circRNA可提高保护作用
为提高疫苗保护作用,研究合成NS1 circRNA,并将等量EDIII-Fc和NS1的circRNA组合成两种不同的配方:EN(LNP)是LNP分别包封两种circRNA;EN(RNA)是LNP包封EDIII-Fc和NS1 circRNA的预混合物。将circRNA疫苗分别肌肉注射到C57BL/6小鼠体内,结果发现两种配方的EDIII-Fc和NS1 circRNA的组合疫苗,与单独circRNA相比,都可更好地保护新生儿免受寨卡病毒引起的症状和脑损伤。

(图3)图3 EDIII-Fc和NS1 circRNA联合单剂量免疫在ZIKV感染新生小鼠模型中的免疫原性和保护作用。
对小鼠进行加强剂量后,EN(LNP)和EN(RNA)有效地抑制了ZIKV引起的脑膜炎症和皮质层状坏死;而EDIII-Fc或NS1 circRNA可大大减少,但不能消除ZIKV引起的脑损伤(图4h)。EDIII-Fc和NS1 circRNA的组合,特别是EN(LNP)配方,有可能提供充分的保护,但需要双剂量。
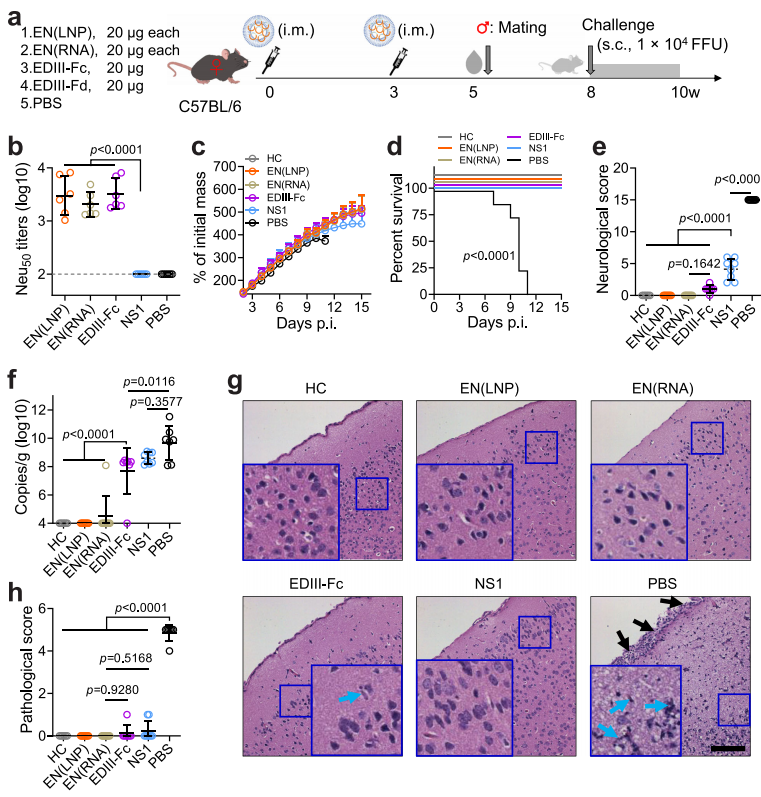
(图4)图4 EDIII-Fc和NS1 circRNA联合双剂量免疫对ZIKV感染新生小鼠模型的免疫原性和保护作用。
四、circRNA免疫不会增强小鼠的DENV2感染
研究建立小鼠适应的DENV2变体,可增强小鼠毒性。研究circRNA苗候选物的ADE效应的评估中发现,EDIII-Fc单独或与NS1联合可引起最小且短暂的DENV反应性抗体,EDIII-Fc单独或与NS1联合,只能引起极少的ADE易感性抗体。这表明,在测试环境中,EN(LNP)免疫不太可能导致小鼠DENV2感染的ADE。
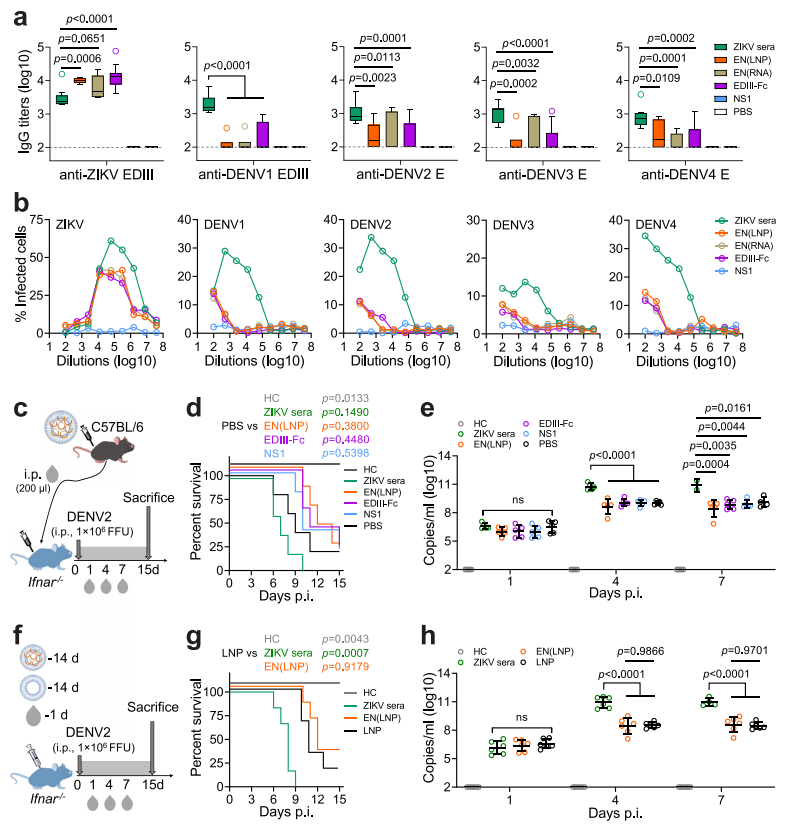
(图5)图5 circRNA原型疫苗在小鼠中的ADE风险。
五、单剂量优化的circRNA疫苗可提供有效的保护
为了提高circRNA疫苗的翻译效率,研究对circRNA进行了优化:使用更高翻译效率的IRES(iHRV-B3),并在上游5’处引入了一个人poly(A)结合蛋白(PABP)的RNA结合基序,在iHRV-B3的IV结构域的近端环处插入了一个eIF4G招募适体(Apt-eIF4G),并在终止密码子的下游3’处添加人α-球蛋白1 (HBA1) mRNA的3 ' UTR(图6a)。这些优化显著提高了蛋白质产量,及circRNA作为疫苗的免疫原性。单剂优化EN(LNP)的母体免疫即可完全保护子代免受寨卡病毒感染,也能有效地保护成年小鼠免受寨卡病毒感染。
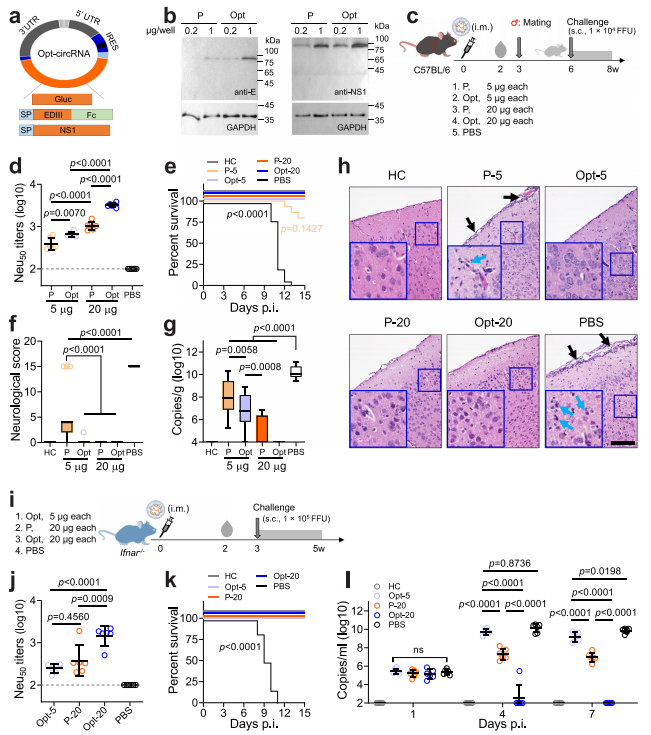
(图6)图6 优化后的EN(LNP)对小鼠的免疫原性和保护效果。
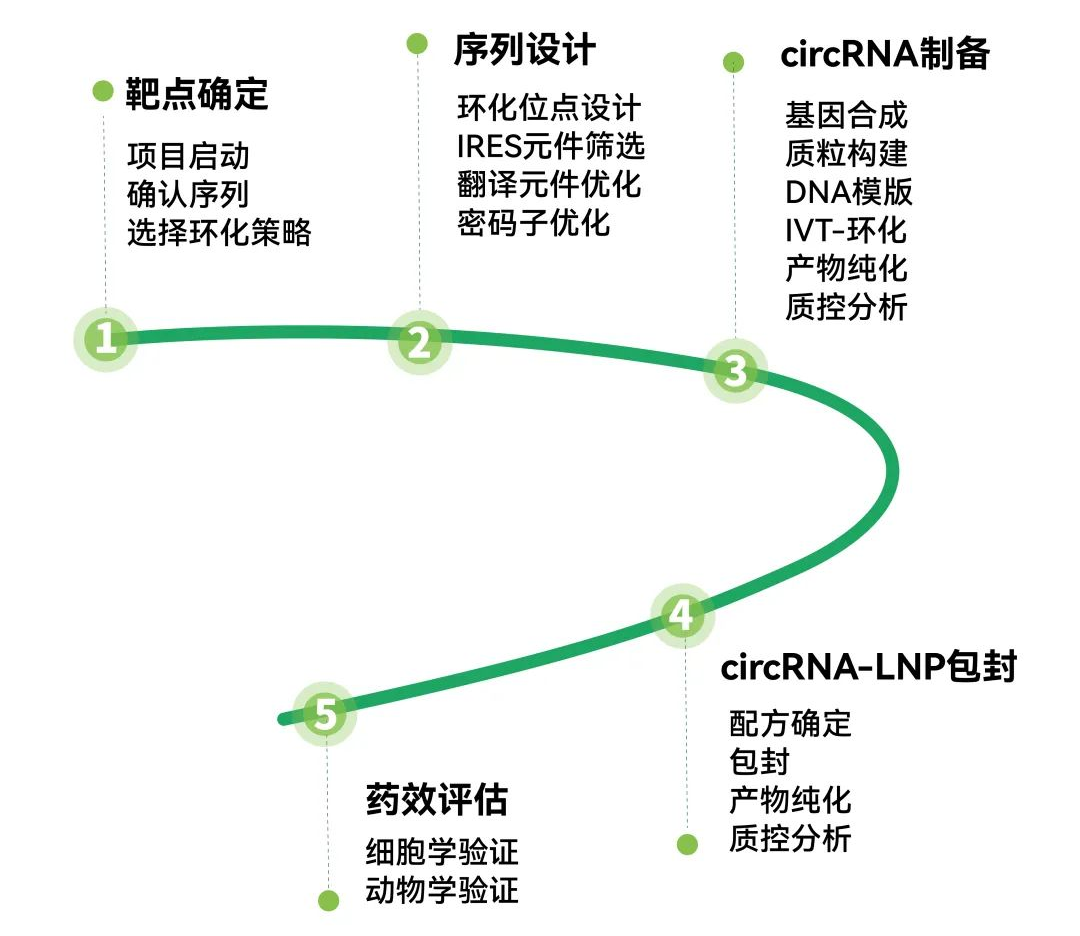
针对早期概念验证和成药性研究,吉赛生物可提供研究级别circRNA体外制备、LNP包封服务和circRNA现货产品,可用于细胞转染、动物实验、药效评估等多领域。
六、优化后的circRNA疫苗引发持久的保护性免疫
相比原型EN(LNP),优化EN(LNP)显著改善了对通过母体被动免疫的幼鼠的保护性,可预防寨卡病毒引起的生长迟缓、死亡率、神经学症状和脑发育迟顿。而且,优化后的EN(LNP)在小鼠中引发了至少持续11周的保护性免疫。
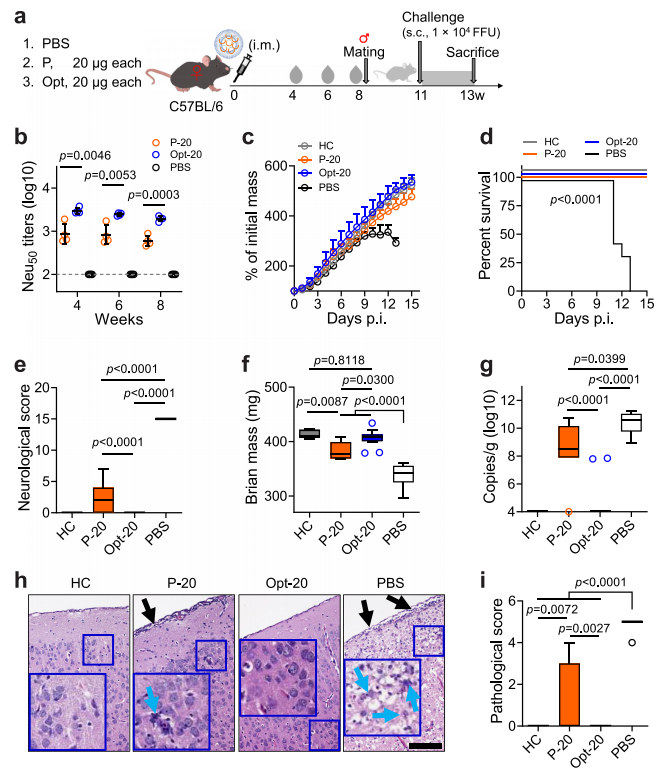
(图7)图7 优化后的EN(LNP)在小鼠体内引发保护性免疫的持久性。
七、circRNA优化不会增加小鼠DENV2 ADE的风险
研究进一步评估优化circRNA引起的ADE风险,结果表明,在测试条件下,优化后的EN(LNP)疫苗或免疫血清不太可能引起DENV2的ADE而促进小鼠的DENV2感染。
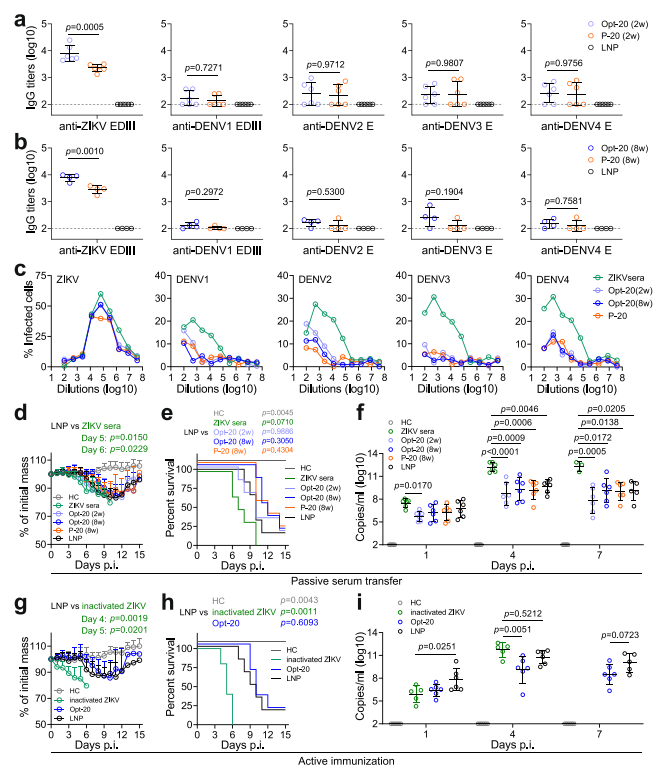
(图8)图8 优化后的EN(LNP)在小鼠中的ADE风险。
结论
综上,基于EDIII-Fc和NS1的circRNA疫苗策略能够有效地保护小鼠免受ZIKV感染,并且不会引起DENV的ADE效应。这项研究不仅提供了一种新的疫苗设计策略,还提供疫苗策略的安全性和有效性的一系列验证方案,并且强调了在疫苗开发中需考虑ADE效应,这对于避免疫苗接种后可能引起的疾病加重风险至关重要。这项研究证明了circRNA作为疫苗平台的潜力,基于EDIII-Fc和NS1 circRNA的疫苗平台为开发安全有效的黄病毒疫苗提供了新的途径,对于控制ZIKV和DENV等黄病毒的传播具有重要意义。
原文链接
https://www.nature.com/articles/s41467-024-53242-0

 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn