
- 首页
- >
- GENESEED
- >
CAR 到底是什么?一文讲清“CAR 家族”与它们的重要地位(附In vivo CAR管线表)
CAR是一种工程化受体,而非一种疗法
CAR(chimeric antigen receptor,嵌合抗原受体)本质上是一种人工设计的受体蛋白。当它在免疫细胞表面表达后,可将对特定分子的结合转化为细胞内信号传导,从而触发相应的激活与效应反应。
所以,CAR 并不等同于CAR-T,也不局限于T细胞。更准确的说法是:CAR提供了一种可在不同免疫细胞上实现的“识别—信号”设计框架;当其分别导入T细胞、NK 细胞或巨噬细胞时,对应形成 CAR-T、CAR-NK、CAR-M 等不同路径。
CAR的结构组成与作用机制
一个典型 CAR 通常可以拆成三段,分别回答三个问题:
外部识别模块:决定“识别谁”
最常见是抗体片段(scFv),也可以用其他配体/受体或结合结构。
连接/跨膜区域:把“外面”和“里面”接起来
它会影响受体的表达稳定性与空间构型。
细胞内信号模块:决定“识别后怎么反应”
经典激活骨架是CD3ζ,常与共刺激结构(如 CD28、4-1BB)组合,用来调节激活强度、扩增动力学与效应持续性等特征。
一句话概括:识别模块决定靶点,信号模块决定应答方式。
CAR 的关键意义在于把“识别—应答”过程拆解为可设计的组合,使不同靶点与信号配置能够被系统比较并持续优化。
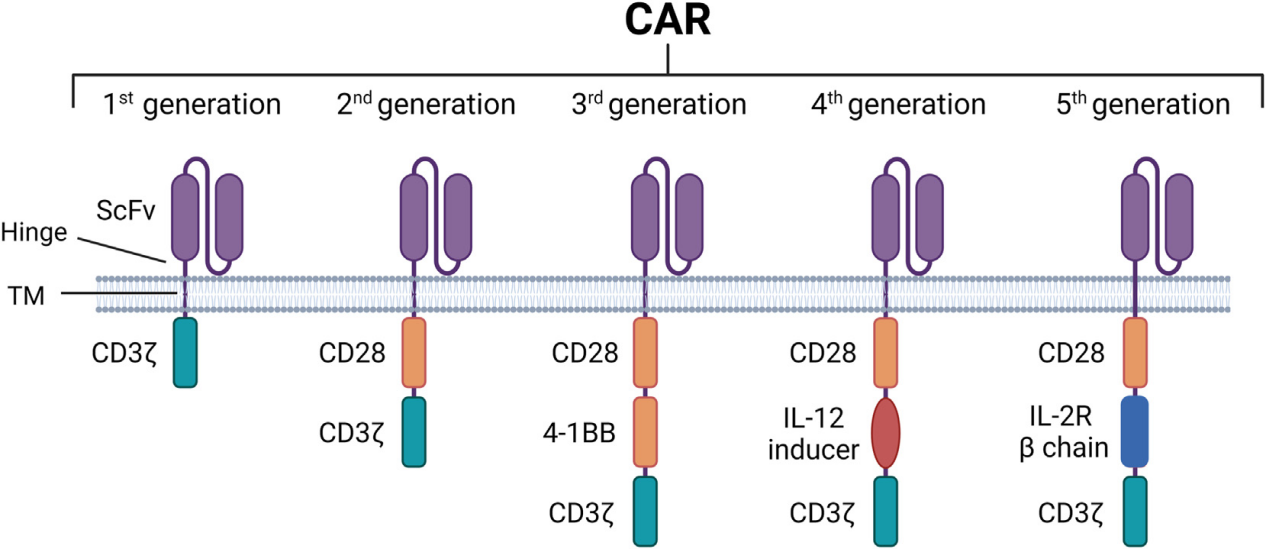
图1 | 不同代CAR-T结构演变示意图[1]
CAR-T 的由来与现实边界
CAR-T的基本思路是将CAR这一“识别—信号”受体导入T细胞,使其在识别肿瘤相关抗原后触发激活与杀伤反应。CAR-T在部分血液肿瘤中已获得较明确的临床证据,因此成为CAR平台中最早进入临床、应用相对成熟的一条路线。
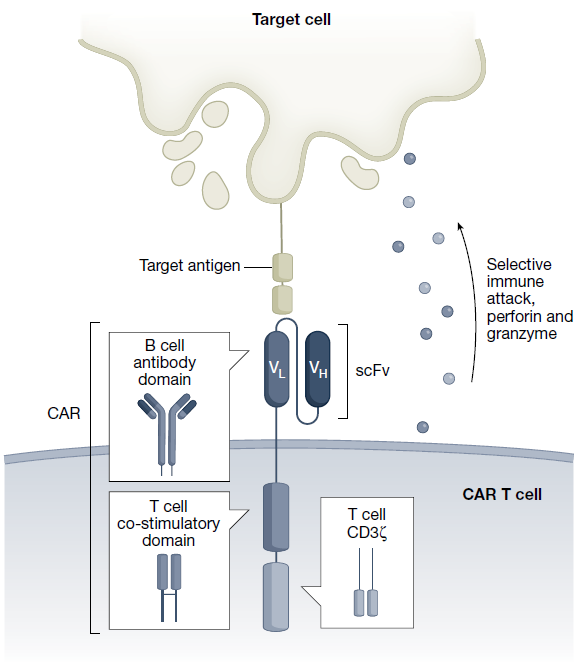
图2 | CAR-T细胞的工程化设计[2]
CAR-T 的推广不只取决于疗效,也受到交付链条的限制:
a.需要采集患者细胞,在体外完成基因导入与扩增,质控通过后再回输;
b.流程长、成本高;
c.不同患者起始细胞质量差异,会影响制备一致性;
d.免疫相关毒性风险,要求完善的监测与处置体系。
这意味着治疗对时间窗口、中心能力和供应链稳定性都有较高要求,也促使研究与产业界持续探索更简化、可标准化的交付方式。
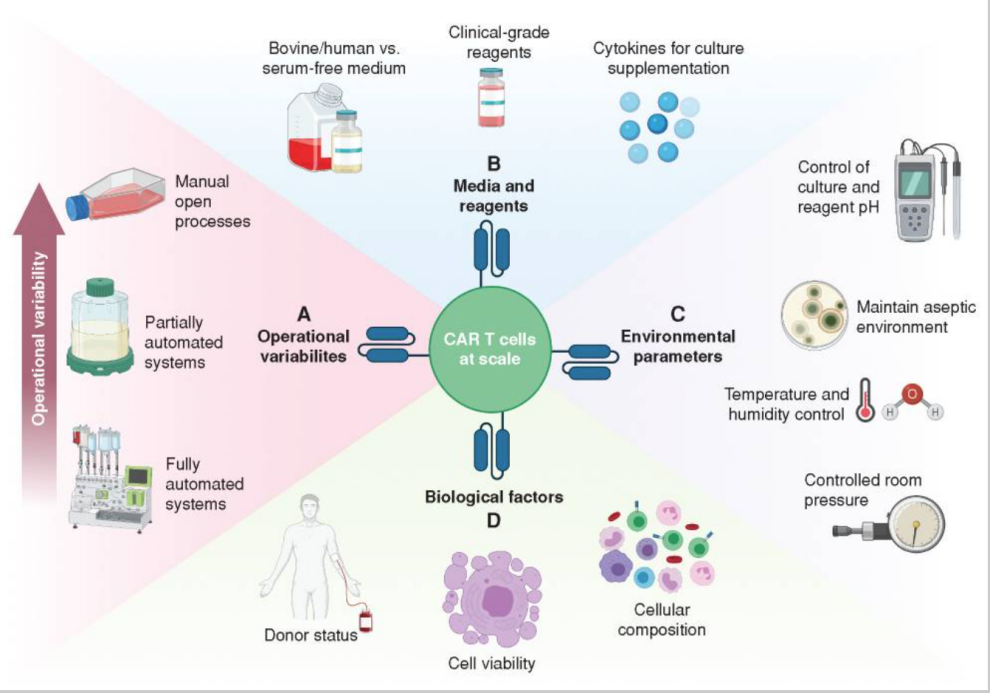
图3 | 规模化 CAR-T 细胞制备的工艺变量[3]
从 CAR-T 到 CAR-NK / CAR-M:
为什么要换细胞底盘
当CAR平台从T细胞延伸到其他免疫细胞时,重点并不是“换个细胞重复同样做法”,而在于不同细胞本身的功能差异是否能带来新的机制路径与适用场景。
CAR-NK:
自然杀伤(NK)细胞具有先天性细胞毒活性,因此相关研究往往讨论其在供给方式、免疫学风险特征及效应机制上的差异;但其体内持续性、功能维持以及制备一致性仍是需要重点解决的问题。
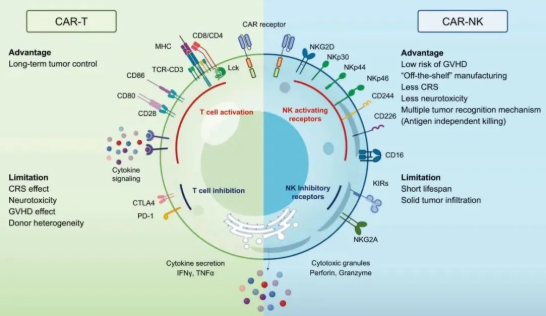
图4 | CAR-T细胞和CAR-NK细胞的对比[4]
CAR-M(CAR-巨噬细胞):
更常与肿瘤微环境相关。巨噬细胞具备吞噬、抗原呈递与免疫调节等功能,因此在实体瘤方向受到关注;但也带来表型可控性、体内行为可预测性以及效力评价体系更复杂等挑战。
总体来看,“CAR 家族”可以理解为同一受体工程思路在不同免疫细胞上的实现;细胞底盘不同,机制侧重与转化难点也会随之改变。因此它们更像是在不同问题上各自更合适的工具,而不是简单的升级/替代关系。
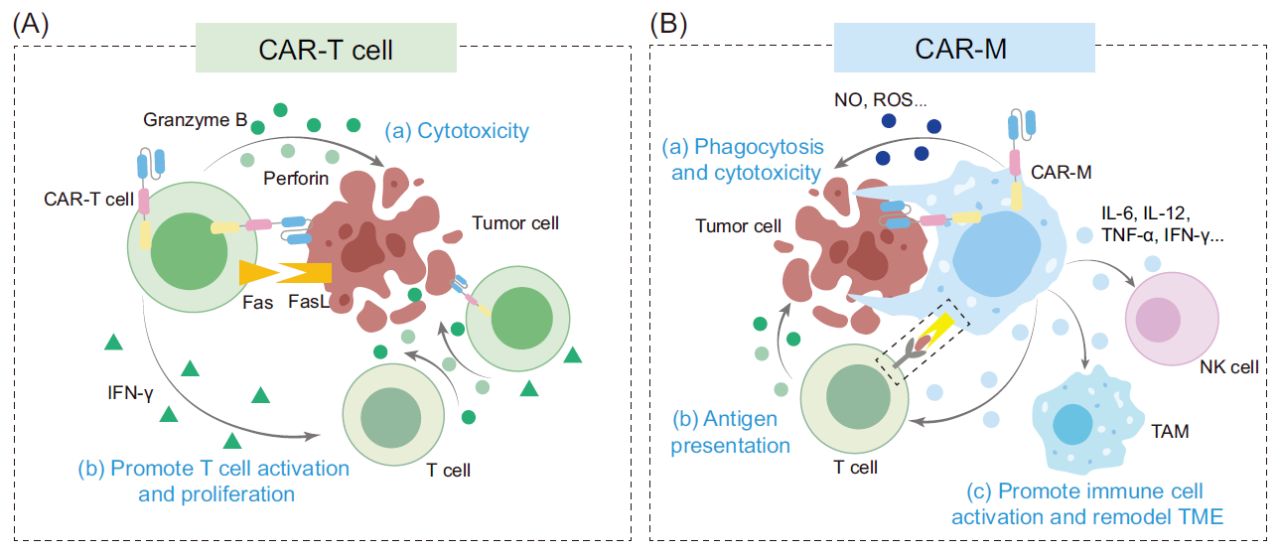
图5 | CAR-T细胞和CAR-M抗肿瘤机制的差异[5]
Ex vivo至In vivo:CAR制备路径的转变
目前,CAR 细胞疗法的临床应用主要依赖体外制备(Ex vivo)模式。但这一模式面临制备周期长、成本高以及供应链复杂等现实限制。因此,直接在体内重编程免疫细胞的In vivo CAR策略,正成为一种极具代表性的研发范式转变。
现阶段,多数In vivo策略依赖mRNA-LNP实现CAR 的瞬时表达,部分项目已进入早期临床。但线性 mRNA 易降解、半衰期短,表达持续性有限,成为疗效稳定性的关键瓶颈。
具备共价闭合结构的circRNA因更稳定、翻译窗口更长,被视为潜在升级方案。尽管目前处于临床前概念验证阶段且递送与规模化生产仍待突破,但其在改善表达持久性和优化药代动力学方面的潜力,正在受到关注。
从mRNA到circRNA,或许不仅是分子形式的迭代,更是RNA疗法设计逻辑的一次进阶。
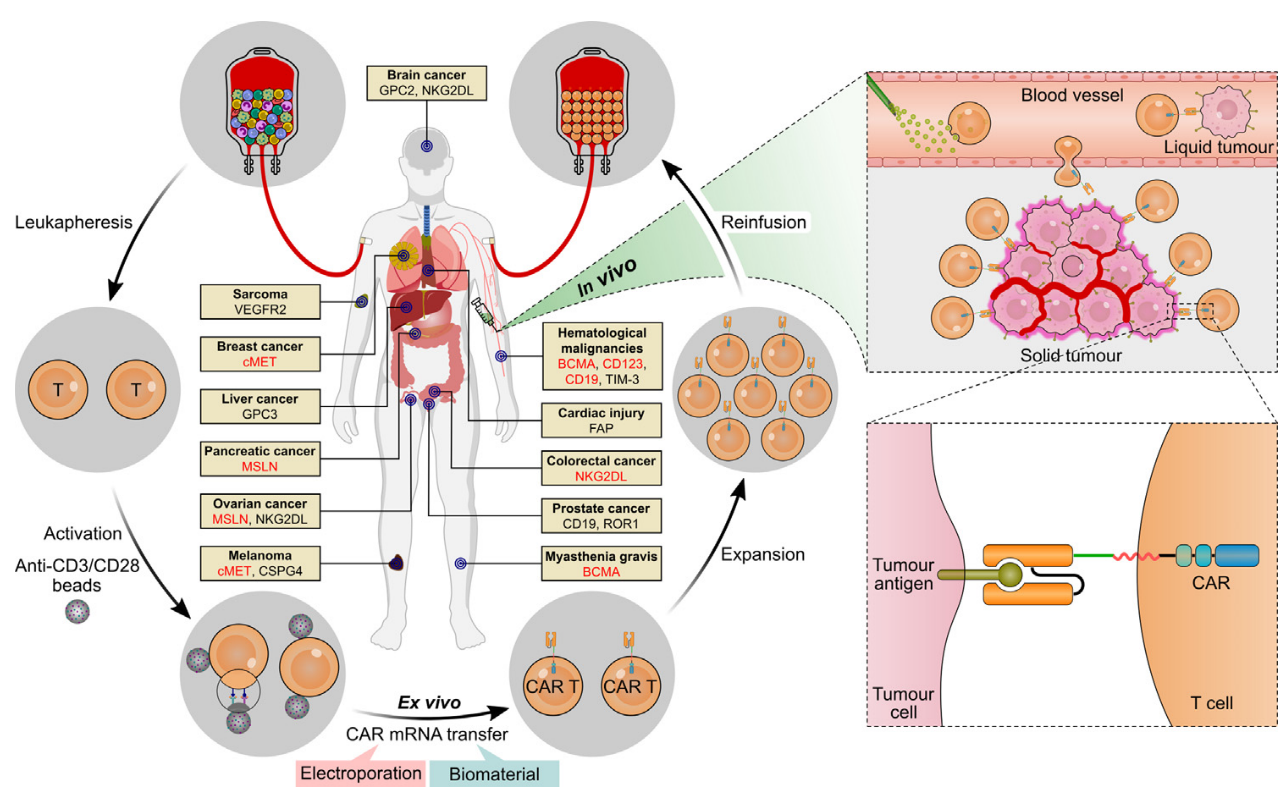
图6 | 基于mRNA的ex vivo CAR-T涉及多个步骤(左),而in vivo CAR-T免除了复杂的流程(右)[6]
全球 In vivo CAR 临床阶段/IIT 管线梳理
LNP-RNA核酸技术路径
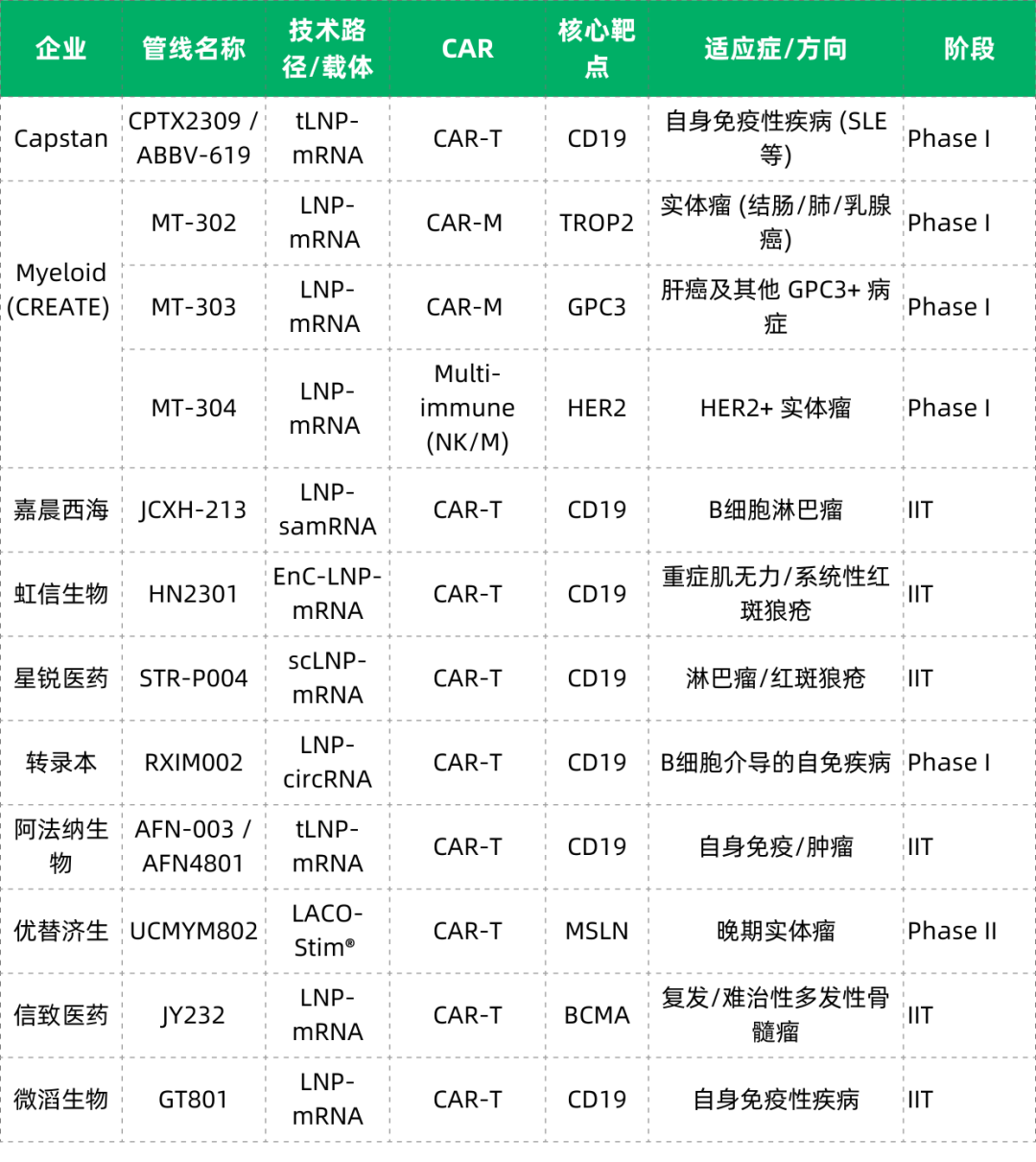
病毒载体基因重编程路径
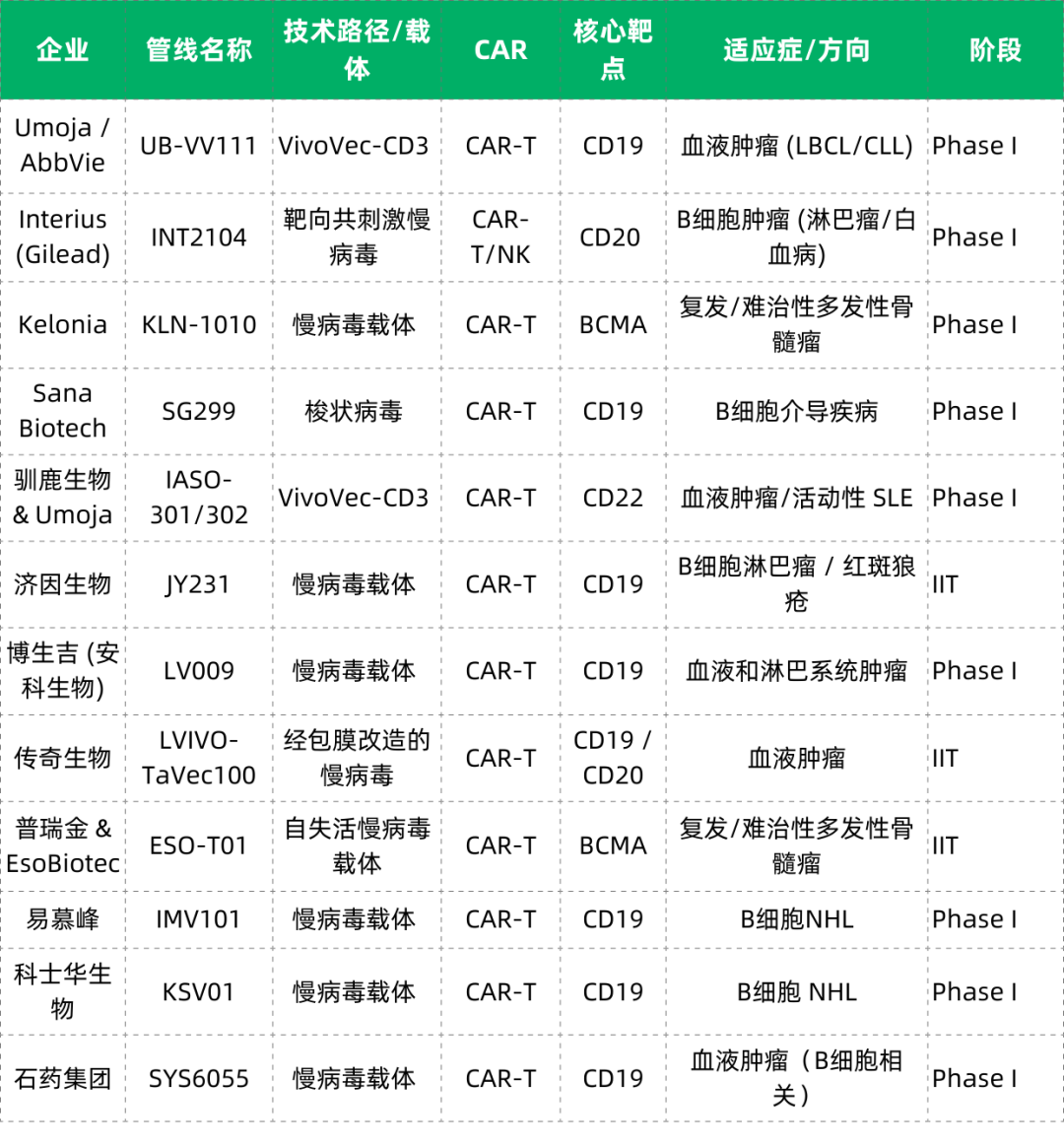
结语
归根结底,CAR 平台的下一步竞争正在变化:从“换什么细胞”转向“如何更稳定、更可规模化地交付到体内”。从 mRNA 到 circRNA,是围绕表达持久性与制造可行性的一次关键探索。
基于这一方向,吉赛生物也在持续完善围绕circRNA 的关键技术与服务能力,聚焦设计优化、环化与纯化工艺、质量分析与规模化制备等环状RNA核心环节,为 in vivo CAR 等前沿探索提供底层支撑。
如果你对circRNA在in vivo CAR等方向的应用感兴趣,欢迎扫码了解吉赛生物的circRNA相关服务与能力。

参考文献
[1]Thuy Anh Bui, et al. Advancements and challenges in developing in vivo CAR T cell therapies for cancer treatment. eBioMedicine 2024;106: 105266. Doi:10. 1016/j.ebiom.2024. 105266
[2]Baker, Daniel J., et al. "CAR T therapy beyond cancer: the evolution of a living drug." Nature, vol. 619, no. 7971, 2023, pp. 707-715.
[3]Abou-El-Enein, Mohamed, et al. "Scalable Manufacturing of CAR T Cells for Cancer Immunotherapy." Blood Cancer Discovery, vol. 2, no. 5, Sept. 2021, pp. 408-422. https://doi.org/10.1158/2643-3230.BCD-21-0084.
[4]Peng, Lei, et al. "CAR-T and CAR-NK as Cellular Cancer Immunotherapy for Solid Tumors." Cellular and Molecular Immunology, vol. 21, no. 10, Oct. 2024, pp. 1089-1108. https://doi.org/10.1038/s41423-024-01207-0.
[5]Wang, Mengru, et al. "Harnessing Chimeric Antigen Receptor Macrophages Against Solid Tumors." Cancer Communications, 2025, https://doi.org/10.1002/cac2.70053.
[6]Wu J, et al. Chimeric antigen receptor therapy meets mRNA technology. Trends Biotechnol. 2024;42(2):228-240.

 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn