
- 首页
- >
- GENESEED
- >
2026开年顶刊新信号:circRNA与m6A修饰正从机制研究走向应用转化
下面,我们就结合这两篇研究,看看这一类机制是如何一步步搭起来,又是如何延伸到下游应用验证的。
发表期刊:Signal Transduction and Targeted Therapy;
发表时间:2026.03;
影响因子:52.7;
关键词: m6A修饰 | RNA-蛋白互作 | 蛋白质棕榈酰化。

研究背景与目的
尽管circRNA已被证实是心脏发育和心血管疾病的关键调节因子,但其在心肌缺血再灌注(I/R)损伤中的具体作用与上游表观调控网络尚未得到充分阐明。该研究旨在系统鉴定I/R损伤中受m6A修饰调控的关键分子(circArhgap26),并深入探究其如何通过直接结合靶蛋白(PKP1),干预该蛋白与转移酶的互作及后续的棕榈酰化修饰。该研究首次揭示了“m6A修饰(表观调控)”与“蛋白质棕榈酰化(翻译后修饰)”双重干预对抗I/R损伤的分子机制,为基于circRNA的心血管精准靶向治疗提供了理论基础。
研究思路与结果
m6A修饰介导的circRNA降解机制
在心肌缺血再灌注(I/R)病理条件下,circArhgap26的表达显著下调。机制研究表明,这种表达下调受上游表观遗传调控:I/R应激诱导m6A阅读蛋白YTHDF2表达上调,而高表达的YTHDF2可特异性识别并结合circArhgap26上的m6A修饰位点,进而加速其降解,从而触发下游病理反应。
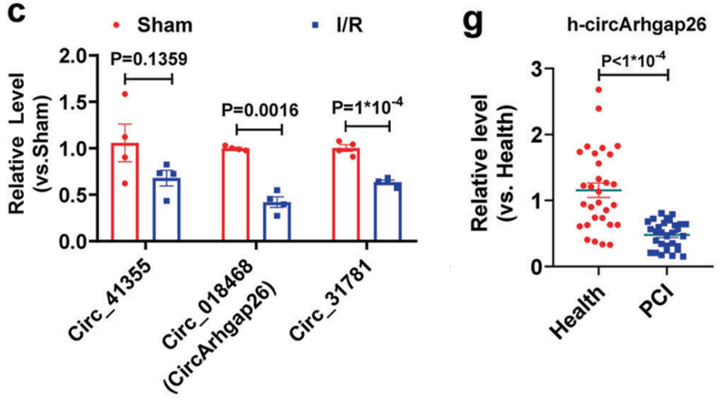
qRT-PCR检测显示,与正常对照组相比,circArhgap26在小鼠I/R心肌组织(图1c)及接受PCI治疗患者的血浆样本(图1g)中均显著下调
circRNA结合靶蛋白的空间遮蔽效应
机制研究进一步发现,circArhgap26通过直接结合PKP1蛋白的ARM1结构域发挥保护作用。在正常生理状态下,这种特异性RNA-蛋白互作可在空间上遮蔽PKP1的关键结合区域,限制其与棕榈酰转移酶ZDHHC1的异常互作,从而维持细胞内蛋白稳态。
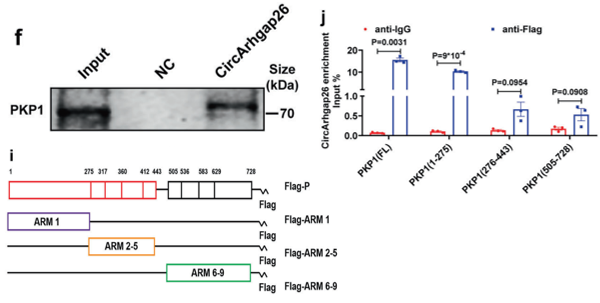
RNA pull-down及截短突变实验(图3f,3i,3j)证实,circArhgap26可特异性结合PKP1蛋白,并定位于其ARM1结构域,从而形成物理遮蔽
蛋白棕榈酰化异常引发的翻译失控与凋亡闭环
随着circArhgap26大量降解,PKP1失去原有保护并暴露关键结合位点。游离的PKP1随后被棕榈酰转移酶ZDHHC1催化发生棕榈酰化修饰,从而阻断其正常降解,导致其在细胞内异常积累。
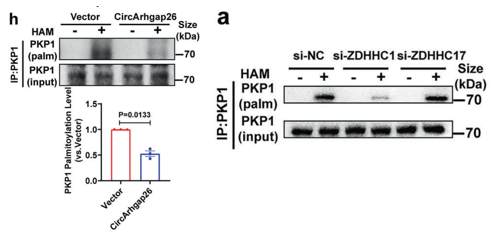
ABE及免疫沉淀实验表明,ZDHHC1可显著增强PKP1的棕榈酰化修饰水平(图6h,7a),从而抑制其正常降解并导致蛋白异常积累
进一步研究表明,积累的PKP1可作用于靶基因APAF1的5'UTR区域,促进其翻译表达;APAF1蛋白异常上调继而激活下游Caspase凋亡级联反应,最终加重心肌损伤。
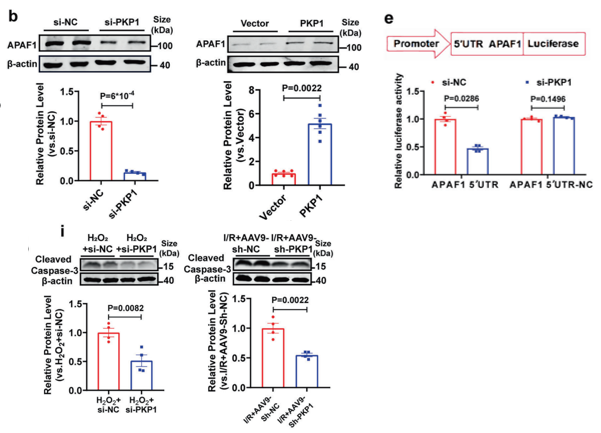
积累的PKP1通过作用于APAF1的5'UTR区域(图8e),促进APAF1蛋白表达(图8b),进而导致Cleaved-Caspase3等凋亡标志物显著增加(图8i)
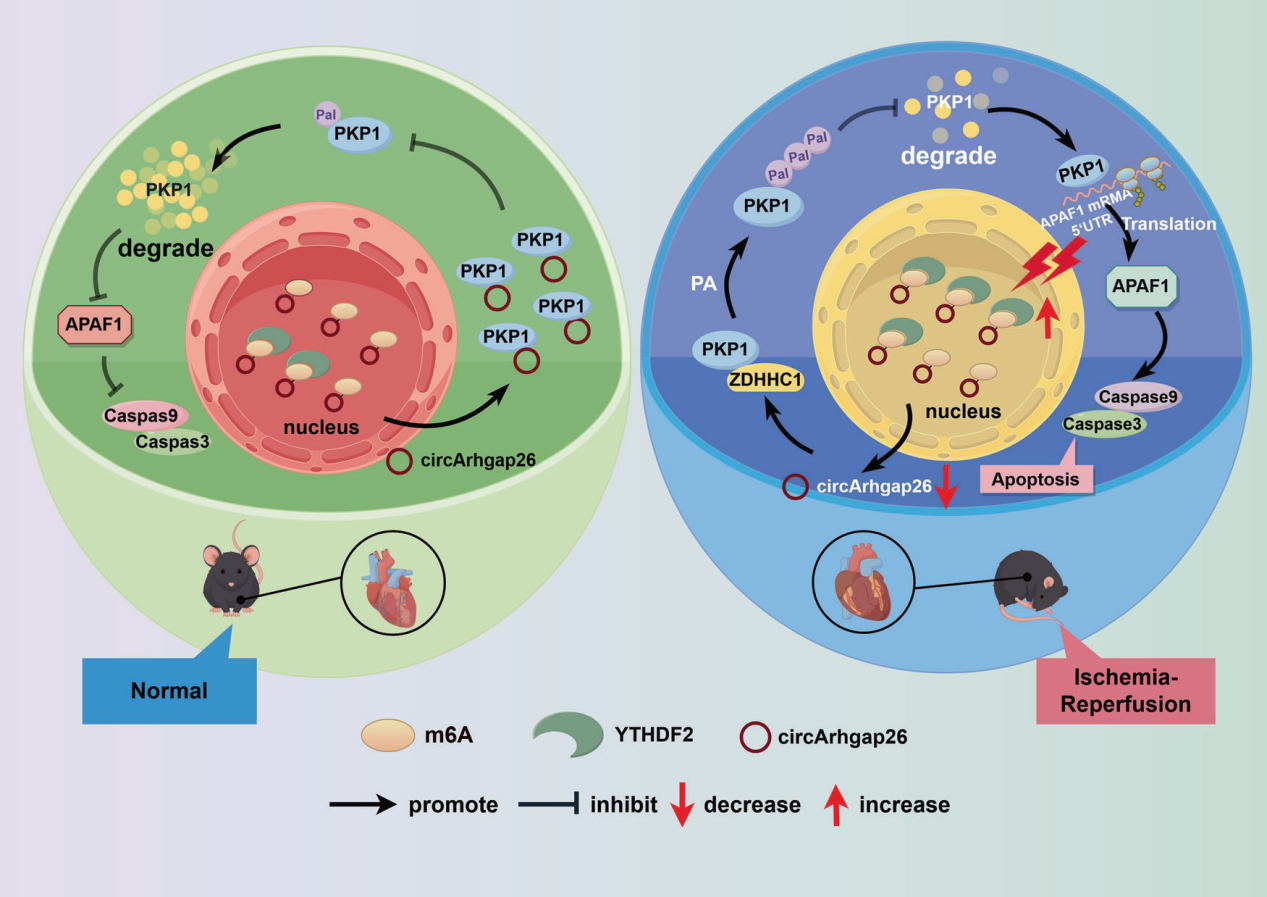
全篇分子机制模式图。 在I/R应激条件下,YTHDF2介导m6A修饰的circArhgap26降解,打破其对PKP1的分子约束;随后,ZDHHC1催化PKP1发生棕榈酰化修饰,抑制其正常降解并导致蛋白异常积累,进而促进APAF1翻译,最终诱导心肌细胞凋亡。
发表期刊:Molecular Biomedicine;
发表时间:2026.03;
影响因子:10.1;
关键词:m6A修饰 | 靶蛋白互作 | 细胞自噬 | 脂质纳米颗粒。

研究背景与目的
m6A修饰已成为骨关节炎(OA)中的重要转录后调控机制,但m6A依赖的circRNA调控在软骨细胞衰老及OA进展中的作用仍缺乏清晰认识。本研究围绕OA相关circRNA——circHIPK2展开,旨在阐明其在m6A-YTHDF2轴调控下的降解机制,解析其通过结合RAB22A影响自噬通路和软骨细胞衰老的分子过程,并进一步评估circHIPK2脂质纳米颗粒递送的干预潜力。
研究思路与结果
m6A修饰介导的circRNA降解机制
在OA病理条件下,软骨组织中整体m6A甲基化水平升高,同时m6A阅读蛋白YTHDF2表达异常上调。机制研究表明,高表达的YTHDF2可识别circHIPK2序列上的m6A修饰位点(GGACU基序),并促进其降解,从而降低circHIPK2的稳定性,导致其在OA进展过程中持续减少。
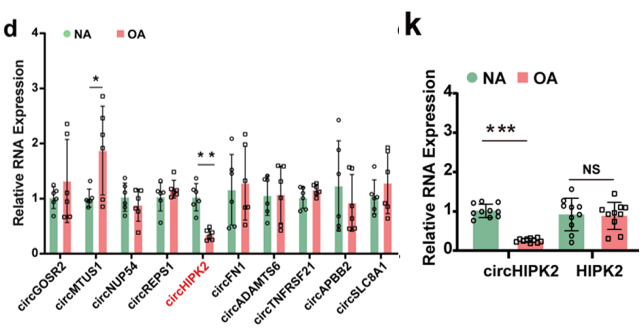
qRT-PCR结果显示,与正常对照组相比,circHIPK2在OA模型中的表达显著下调(图1d,1k)
circRNA直接结合靶蛋白的空间阻断作用
机制研究表明,circHIPK2可通过直接的RNA-protein互作发挥软骨保护作用。在正常状态下,circHIPK2的特定核苷酸位点(G511)可特异性结合RAB22A的核心氨基酸残基(R76),从而在空间上形成阻断作用,限制RAB22A与PI3K的异常结合。
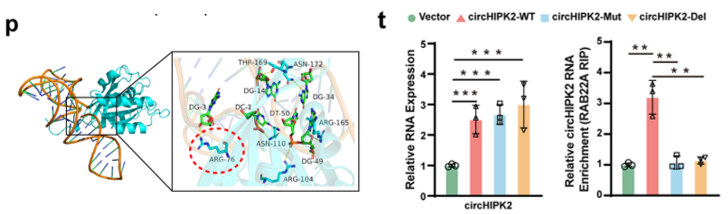
结构预测及突变验证实验(图5p,5t)证实,circHIPK2可结合RAB22A蛋白的特定位点,从而形成空间阻断作用
自噬通路失衡诱发衰老与LNP纳米递送干预
随着circHIPK2大量降解,RAB22A失去原有约束并增强与PI3K的结合,进而异常激活PI3K-AKT-mTOR信号通路,导致软骨细胞自噬流受损,最终加速细胞衰老及OA进展。
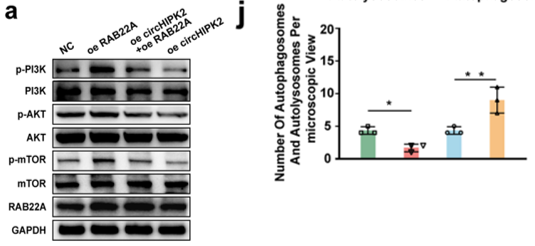
蛋白印迹等实验(图6a,6j)显示,circHIPK2缺失后,游离的RAB22A异常激活PI3K-AKT-mTOR信号通路,导致软骨细胞自噬流受损
基于上述机制,研究团队开发了包封circHIPK2的脂质纳米颗粒(LNP),通过关节腔局部注射实现了circHIPK2在体内的长效、稳定递送。进一步研究表明,该策略可显著恢复软骨细胞自噬能力,并缓解OA小鼠的关节退变表型。
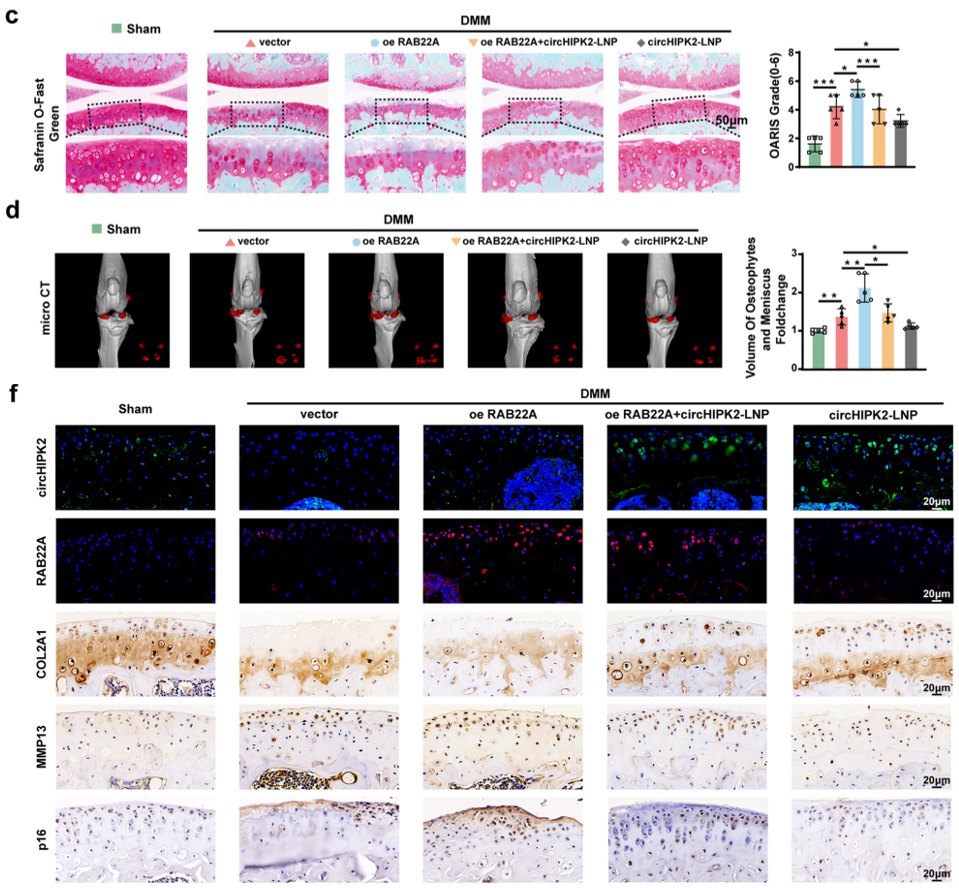
关节腔局部注射LNP后,小鼠软骨组织病理染色(图7c)及相关评分(图7d,7f)均显示,OA病理损伤明显缓解,软骨退变得到改善
小结
尽管上述两项研究分属不同疾病领域,但其背后的调控逻辑却呈现出高度一致的共性:都不是停留在机制描述本身,而是进一步延伸到了蛋白功能失衡、疾病进展乃至体内干预验证。这也提示我们,circRNA相关研究正在从单一机制解析走向更完整的应用转化链条。
对于疾病相关的保护性非编码RNA研究,这两篇文献呈现出一条值得关注的共性路径:
从表达变化追溯上游调控来源
不再停留于“发现某个circRNA下调”,而是进一步追问其为何下调,并将其与m6A修饰及YTHDF2介导的降解联系起来,从而提升研究的完整性与解释力。
从ceRNA假说延伸到RNA-蛋白直接互作
相比传统miRNA海绵模型,这类研究更进一步揭示了circRNA可通过直接结合靶蛋白、形成空间阻断或功能约束,进而影响蛋白修饰、翻译调控或信号转导。
从分子机制闭环走向体内干预验证
高水平研究不仅需要完成机制闭环,更强调其是否具备干预潜力。无论是心血管中的精准治疗启示,还是骨关节炎中的LNP递送验证,都体现了基础研究向转化应用延展的趋势。
◆ ◆ ◆ ◆
吉赛生物
助力环状RNA研究从机制解析走向应用转化
◆ ◆ ◆ ◆
高质量的课题构架,离不开扎实的实验数据支持。吉赛生物深耕环状RNA领域多年,致力于为您提供全链条技术支持,助力您在表观遗传筛选、机制互作解析及体内验证等方面的深入研究:
组学测序服务:提供高分辨率circRNA-seq和Ribo-seq(翻译组测序),精准捕捉circRNA与翻译的关系。
深层机制互作解析:提供专业的RNA Pull-down、RIP、ChIP试剂盒及高通量质谱分析服务,助力验证circRNA的靶蛋白和互作网络。
功能与转化模型:提供circRNA定制载体构建、LNP靶向递送技术咨询,推动环状RNA的临床转化应用。
无论是科研探索还是应用研究,吉赛生物都能为您的项目提供定制化解决方案,助力科研成果快速转化。如有相关研究需求,欢迎联系吉赛生物,获取专属定制方案!
参考文献:
[1] Zhang, MY., Ji, DN., Qi, WY. et al. M6A-modified circArhgap26 attenuates cardiac ischemia–reperfusion injury by suppressing plakophilin-1 palmitoylation. Signal Transduct Target Ther 11, 99 (2026).
[2] Long, D., Lin, Z., Li, Z. et al. YTH N6-methyladenosine RNA binding protein 2 mediated m6A modification of circHIPK2 promotes cellular senescence and osteoarthritis progression by inhibiting autophagy. Mol Biomed 7, 39 (2026).

 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn